Bir önceki konumuzda saf maddeler konusuna değinmiştik. Şimdi ise Karışımlar ve Karışımların Ayrıştırılması konusuna bir göz atalım.
KARIŞIMLAR
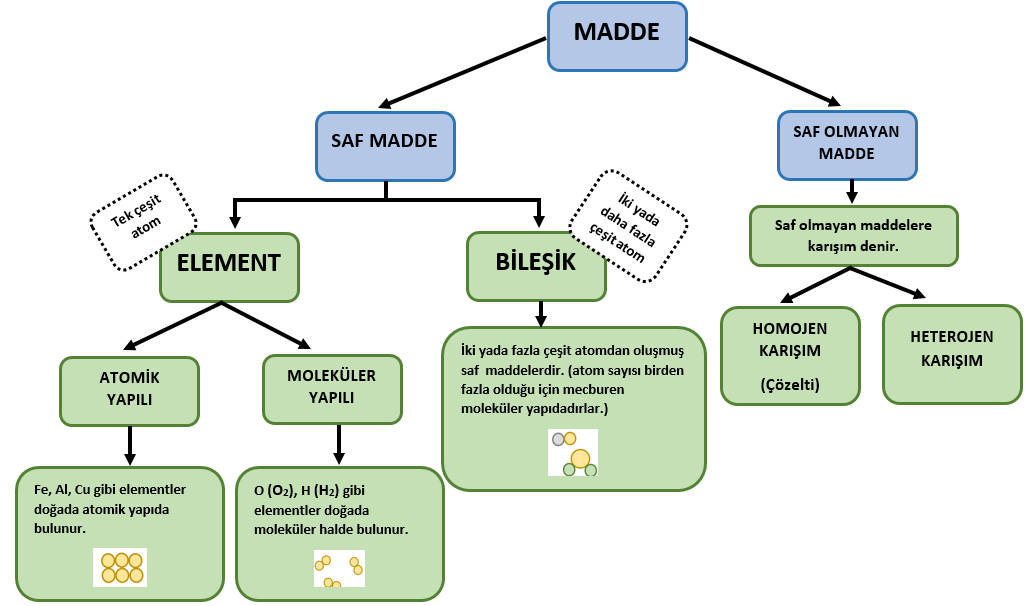
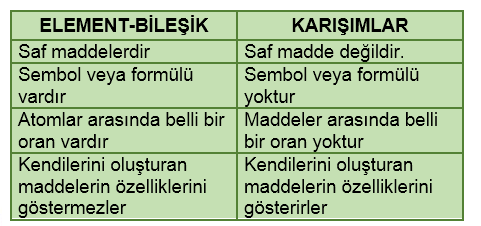
Birden çok maddenin kimyasal bağ oluşturmadan bir araya gelmesiyle oluşan maddelere karışım denir. Karışımlar saf madde değildir.
Şeker ile su, su ile zeytinyağı gibi maddeler karıştırıldığında oluşan maddeler karışımdır.
Karışımlar içerisinde bulunan maddenin görünümüne göre homojen ve heterejon olmak üzere ikiye ayrılır.
Homojen Karışım (Çözelti):
Tuzlu su, şekerli su, kolonya, deniz suyu, hava homojen karışımdır. Yani karışımı oluşturan maddeler karışımın her tarafına eşit olarak dağılmıştır. Bir bardağın içerisinde su ve tuzu karıştırdığımız zaman bardağın neresinden bakarsak bakalım aynı şeyi görürüz. Homojen karışımın diğer adı çözeltidir.
Heterojen Karışımlar:
Kumlu su, zeytinyağı-su, ayran gibi karışımlar heterojen karışımlardır. Yani karışımı oluşturan maddeler karışımın her tarafına eşit olarak dağılmamıştır. Bir bardakta zeytin yağı ve suyu karıştırdığımızda bardağın farklı yerlerinden bakıldığı aynı maddeyi göremeyeceğiz. Aynı şekilde ayranı ele alırsak. Su ve yoğurdu karıştırdığımızda ilk anlık homojen bir karışım elde etmiş oluruz. Ancak biraz beklediğimiz zaman yoğurt dipte çökerken su yukarda kalacaktır.
Çözeltiler, çözücü ve çözünenden oluşmuştur. Miktarı fazla olan çözücü, miktarı az olan ise çözünendir.

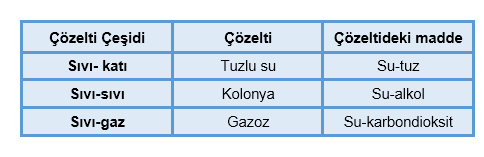
Sıvı çözeltiler; sıvı-sıvı, sıvı-katı ve sıvı-gaz olmak üzere üç çeşidi bulunmaktadır.
Çözünme:
Çözünen madde taneciklerinin birbirinden ayrılarak çözücü madde tanecikleri arasında dağılmasına çözünme denir. Çözünen maddenin tanecikleri moleküler halde çözülmüşse elektrik akımını iletmez. Ancak çözünen maddenin tanecikleri iyonlar şeklinde çözünmüşse elektrik akımını iletir. Elektik akımını ileten çözeltilere elektrolit çözelti denir.
 Çözeltinin elektrik akımını iletmesi iyon halinde çözünen taneciklerin hareketinden dolayıdır.
Çözeltinin elektrik akımını iletmesi iyon halinde çözünen taneciklerin hareketinden dolayıdır.
Limonlu su, tuzlu su, yağmur suları, sirkeli su elektrik akımını iletir.
Çözünme Hızına Etki Eden Faktörler
Tanecik boyutunun küçültülmesi ve sıcaklığın artırılması çözünme hızını artırır.
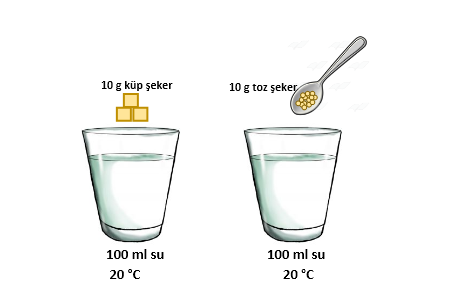 Eşit miktardaki küp ve toz şeker şekildeki bardaklara atıldığında toz şeker daha çabuk çözünür.
Eşit miktardaki küp ve toz şeker şekildeki bardaklara atıldığında toz şeker daha çabuk çözünür.
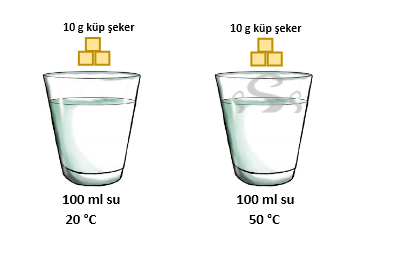 Eşit miktarda küp şeker sıcaklıkları farklı bardaklara atıldığında sıcaklığı fazla olan (50 °C) bardakta çözünme daha çabuk gerçekleşir.
Eşit miktarda küp şeker sıcaklıkları farklı bardaklara atıldığında sıcaklığı fazla olan (50 °C) bardakta çözünme daha çabuk gerçekleşir.

İçerisinde eşit miktarda çay bulunan fincanlara eşit büyüklükte farklı sayıda küp şekerler atılıyor. Üç tane küp şeker atılan çay diğerlerine göre daha tatlı olur.
Başka bir çözeltiye göre çözünen madde oranı fazla olan çözeltiye derişik, çözünen madde oranı az olan çözeltiye ise seyreltik çözelti denir.
Fincanlarda ;
Çay: Çözücü madde
Küp şeker: Çözünen maddedir.
3 fincanı karşılaştırdığımızda ilk fincanda 3 tane küp şeker çözündüğünden yani çözünen madde miktarı fazla olduğundan derişik; üçüncü fincanda 1 tane şeker çözündüğünden yani çözünen madde miktarı az olduğundan seyreltiktir.
Var olan çözeltileri bazı işlemler uygulayarak derişik veya seyreltik yapılabilir.

Çözücü ekleme, seyreltik çözelti
Bir çözeltiye çözücü madde eklediğimizde çözünen madde miktarı değişmez fakat oranı azalır. Çözelti seyreltik hale gelir.

Çözünen ekleme, derişik çözelti
Bir çözeltiye çözünen madde eklediğimizde madde miktarı ve oranı artar. Çözelti derişik hale gelir.

Çözücü buharlaştırma, derişik çözelti
Bir çözeltiden çözücü buharlaştırıldığında çözünen madde miktarı değişmez. Ancak çözücü miktarı azaldığından çözünen madde oranı artar, çözelti derişik hale gelir.
Karışımların Ayrıştırılması
1.Buharlaştırma yöntemi
Katı-sıvı homojen karışımları ayırmak için kullanılan bir
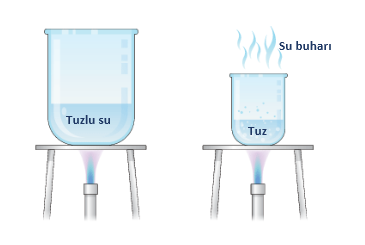
Örneğin; Tuzlu suyu buharlaştırdığımızda su(çözücü) ortamdan uzaklaşacaktır ve ortamda tuz (çözünen) madde kalacaktır. Günlük hayatta buharlaştırma yöntemini salça, pekmez, reçel yapımında sıkça kullanırız.
2.Ayrımsal Damıtma
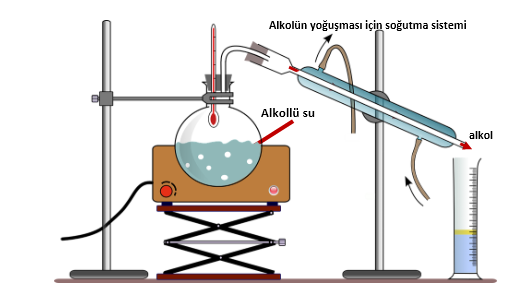
Sıvı-sıvı homojen karışımları ayırmak için kullanılan bir yöntemdir. Bu yöntemde sıvıların kaynama sıcaklıklarından yararlanılmıştır.
Örneğin; alkollü su karışımında alkolün kaynama noktası 76 °C, suyun kaynama noktası ise 100 °C’dir.
Çözeltiyi ısıttığımız zaman ayrımsal damıtmada ilk olarak kaynama noktası düşük olan alkol buharlaşacak sonra tekrardan sıvı hale getirilerek bir kapta toplanacaktır. Alkol tamamen buharlaştığında bir kapta su diğer kapta alkol bulunacaktır.
Petrol refinerilerde motorin, benzin gibi yakıtlar ayrımsal damıtma yöntemiyle elde edilir.
3.Yoğunluk Farkından Yararlanarak Karışımları Ayırma Yöntemi
1. Yoğunlukları farkı iki katı madde:
Yoğunlukları farklı olan iki katı madde karışımı suya atıldığında yoğunluğu küçük olan katı suda yüzerken, yoğunluğu büyük olan katı suda batar. Uygun bir süzgeçle samanlar alınır. Kalan kum-su karışımı süzülerek veya buharlaştırılarak ayrılır.
2.Heterojen sıvı-sıvı karışımlar
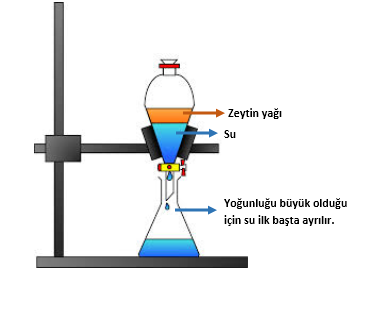
Yoğunlukları farklı olan iki sıvı karıştırıldığında heterojen bir karışım elde edilir. Yoğunluğu fazla olan sıvı dipte olurken yoğunluğu küçük olan sıvı yüzer. Bu iki sıvıyı ayırma hunisi ile ayırabiliriz. Örneğin; zeytinyağı-su karışımı ayırma hunisi ile ayrılırken karışımdan önce su sonra da zeytinyağı elde edilir.
Böylelikle Karışımlar ve Ayrıştırılması konusunu tamamladık. Umuyoruz ki bu konuyu yararlı bulmuşsunuzdur. Güncel konular için facebook , google+ ve twitter üzerinden bizi takip edebilirsiniz.
 Bizlere destek olmak için sayfanın en altına yorum yapabilir veya sosyal medyadan çalışmalarımızı paylaşabilirsiniz. Geri bildirimleriniz bizim için önemli. Tekrar görüşmek üzere.
Bizlere destek olmak için sayfanın en altına yorum yapabilir veya sosyal medyadan çalışmalarımızı paylaşabilirsiniz. Geri bildirimleriniz bizim için önemli. Tekrar görüşmek üzere.




oldukça kapsamlı,faydalı bilgilerle dolu kaliteli çalışmalar.
benim için çok yararlı oldu, teşekkür ederim.
Yüce Mevla’ya emanet olasınız, hayırlı işler, veselam.