Doğada bulunan elementlerin, benzer ve farklı özelliklerine göre gruplanıp sıralandığı sisteme Periyodik Tablo denir.
Periyodik Tablo ile elementler belli özelliklere göre gruplandığı için;
- Elementler üzerinde bilimsel çalışma yapma yapmak daha kolay olur.
- Bir elementi periyodik tabloda daha kolay bulabiliriz.
PERİYODİK TABLONUN ÖZELLİKLERİ
- Elementler periyodik tabloda artan atom numaralarına (proton sayılarına) göre sıralanırlar.
- Aynı grupta olan (alt alta dizilen) elementler benzer fiziksel ve kimyasal özellikler gösterirler.
- Periyodik tabloda bir elementin adı, sembolü, atom numarası, kütle numarası gibi bir çok özelliği yer alır.
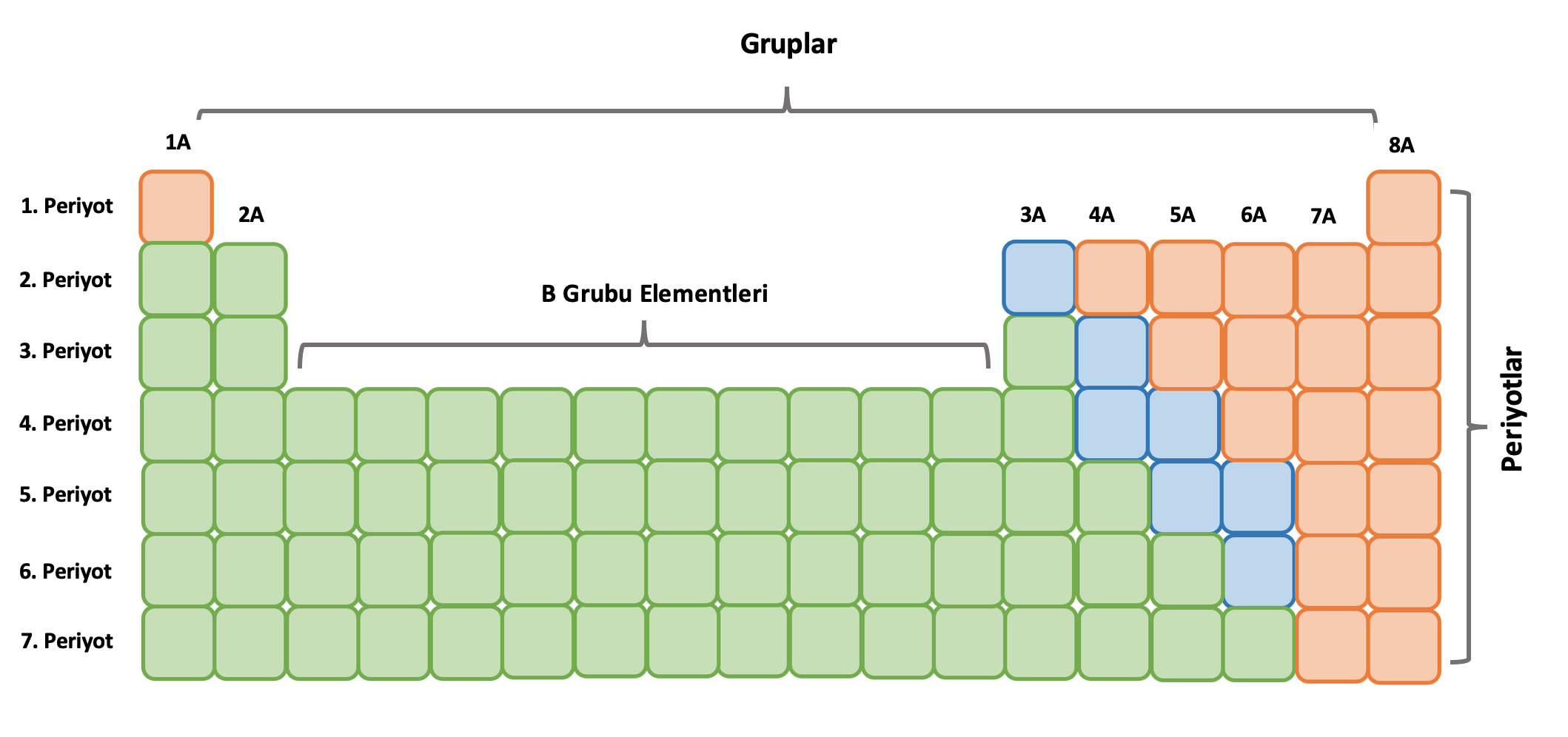
- Periyodik tabloda;
5. Periyodik tabloda; 7 tane periyot, 18 tane grup vardır. Bu 18 grubun 8 tanesi A grubu, 10 tanesi B grubudur.
6. Bazı grupların özel isimleri vardır:

Periyodik Tabloda Yer Bulma:
KURAL:
1.Elementin nötr halinin elektron dağılımı aşağıdaki kurala göre yapılır.
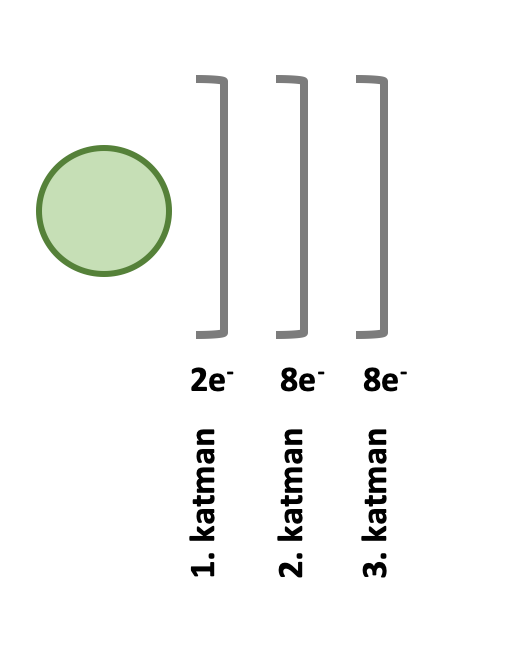
2. Elektron dağılımında,
- Katman Sayısı = Periyot Numarasını
- Son Katmandaki Elektron Sayısı = Grup Numarasını verir.
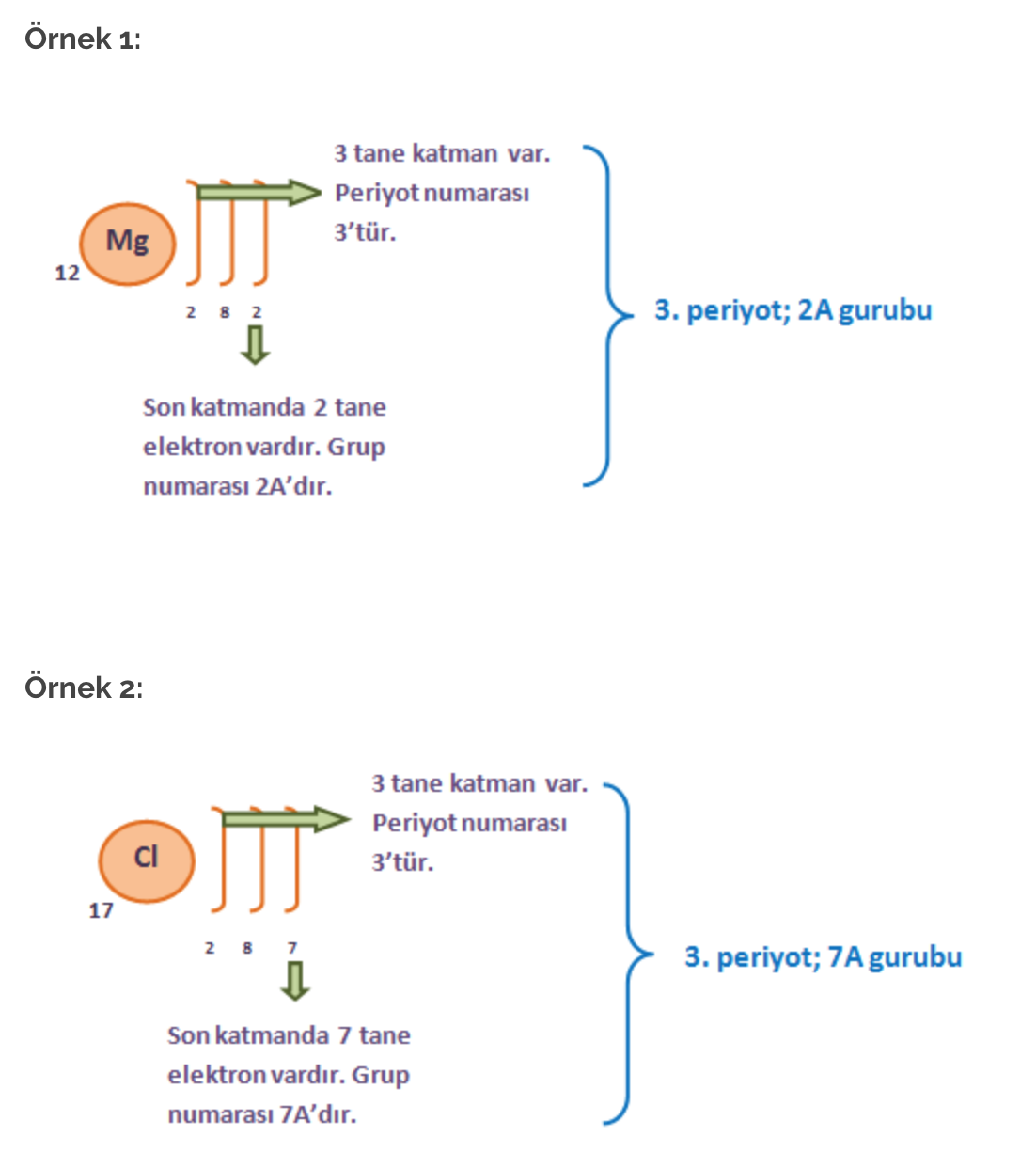
Periyodik Tabloda Elementlerin Sınıflandırılması
1. Metaller:
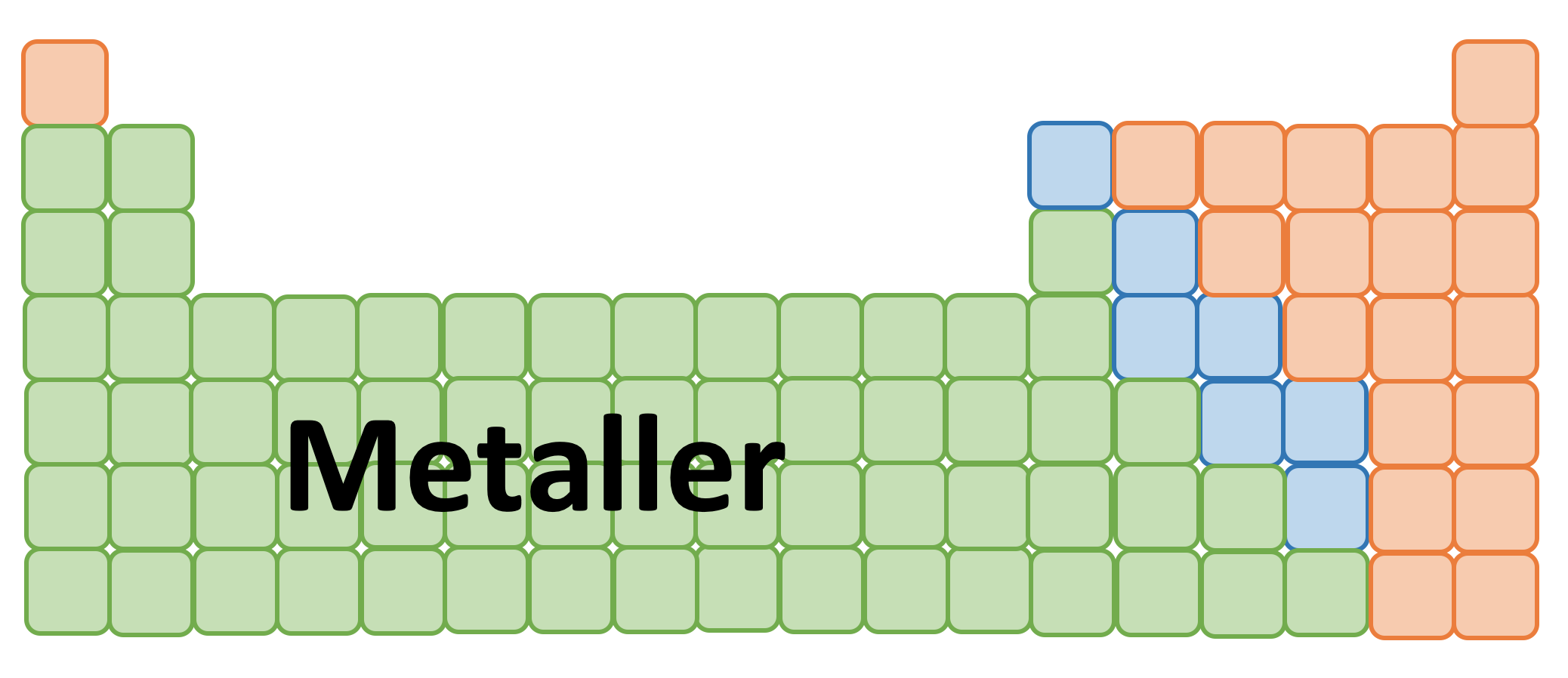
- Yandaki resimde yeşil renk ile gösterilen elementlerdir.
- Genellikle periyodik tablonun sol tarafına gruplanmışlardır.
- Son katmanlarındaki elektron sayısı 1, 2 veya 3’tür. (Elektron dağılımı yapıldığında son katmandaki elektron sayısı bu sayılardan biri ise o element metaldir.)
- Tel ve levha haline getirilebilirler. (Şekil verilebilirler.)
- Isı ve elektriği iyi iletirler.
- Parlaktırlar.
- Oda koşullarında katıdırlar.
- Civa hariç !
- Civa oda sıcaklığında sıvı olan tek metaldir.
- Kendi aralarında bileşik oluşturamazlar. Ametaller ile bileşik oluşturabilirler.
- Atomik yapıdadırlar.
- Erime ve kaynama noktaları yüksektir.
2. Ametaller:
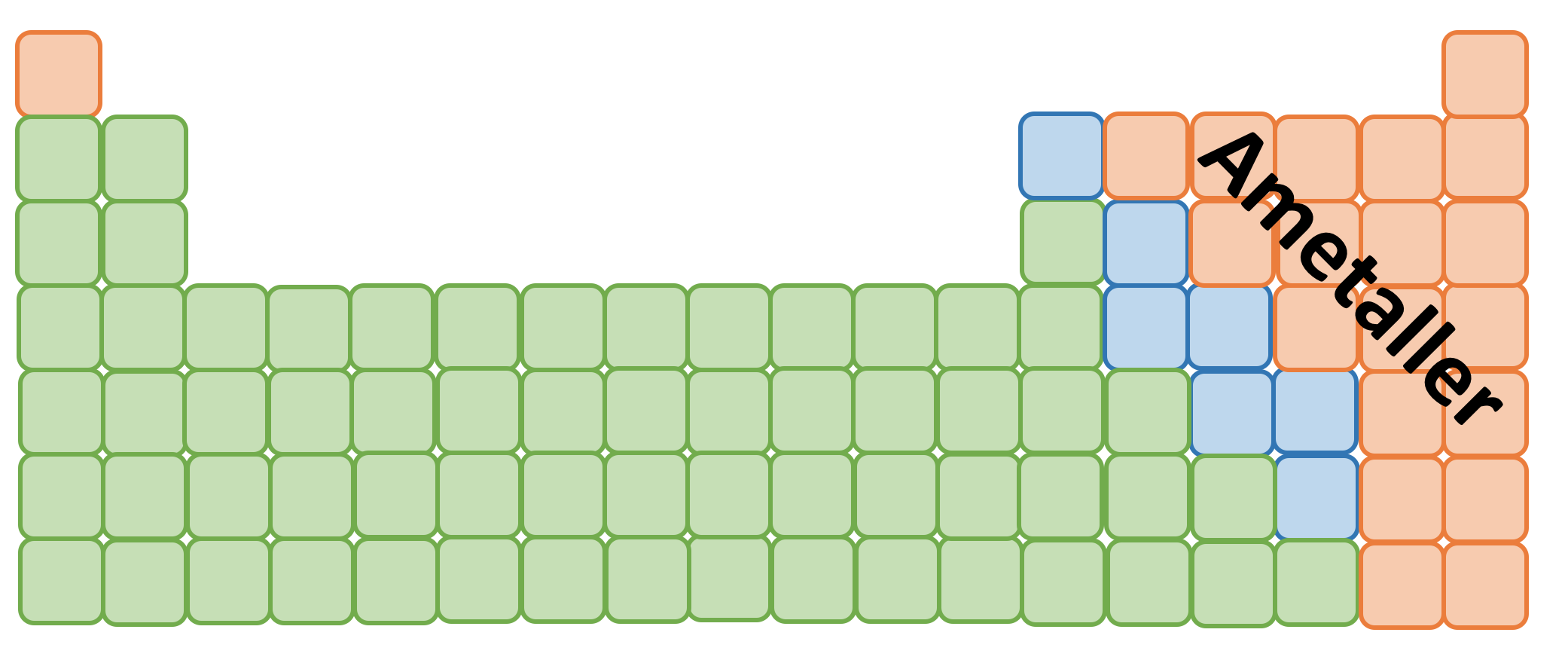
- Yandaki resimde turuncu ile gösterilen elementlerdir.
- Genellikle periyodik tablonun sağ tarafına gruplanmışlardır.
- Hidrojen (H) hariç!
- Hidrojen en solda 1.periyot 1A grubunda bulunur.
- Son katmanlarındaki elektron sayısı 5, 6 veya 7’dir. (Elektron dağılımı yapıldığında son katmandaki elektron sayısı bu sayılardan biri ise o element ametaldir.)
- Tel ve levha haline getirilemezler.
- Isı ve elektiriği iyi iletmezler yada hiç iletemezler.
- Mattırlar.
- Oda koşullarında katı, sıvı yada gaz halde bulunabilirler.
- Kendi aralarında ve metallerle bileşik oluşturabilirler.
- Molekül yapıdadırlar.
Soygazlar:
- 8A grubu elementleridir.
- Ametallerin içinde yer alan, farklı özelliklere sahip özel bir gruptur.
- Oda sıcaklığında hepsi gaz haldedir.
- Karalı yapıya sahiptirler (Elektron dağılımı yapıldığında katmanlarının hepsi dolar.)
- Bileşik oluşturmazlar ve kimyasal reaksiyona girmezler.
- Tek atomludurlar.
- Isı ve elektiriği iletmezler.
3. Yarı Metaller:
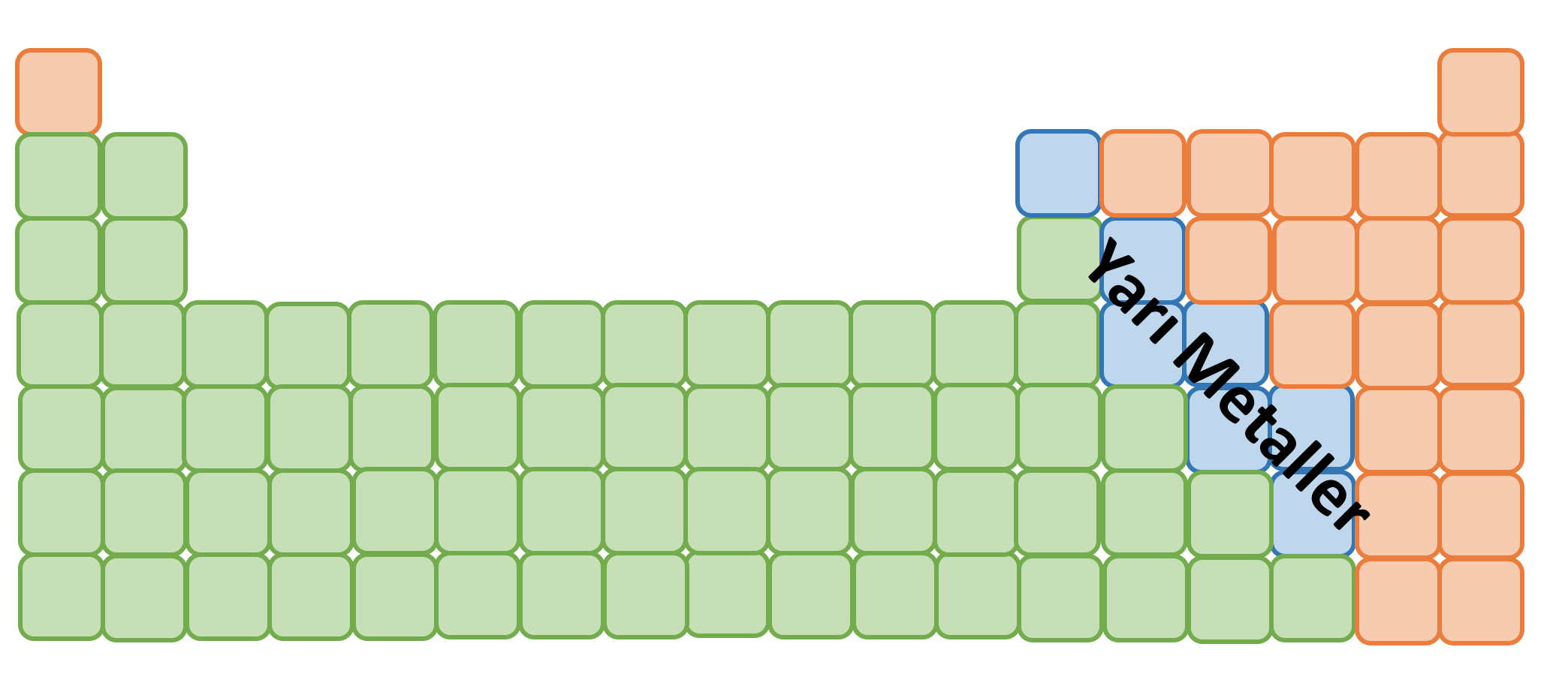
- Periyodik tabloda metal ve ametaller arasında bulunurlar.
- Bor (B) ve Silisyum (Si) ilk 20 element içindeki yarı metallerdir.
- Yarı metallerin; fiziksel özellikleri metallere, kimyasal özellikleri ametallere benzer.
- Parlak yada mat olabilirler.
- Oda koşullarında katı haldedirler.
- Isı ve elektriği metallere göre az, ametallere göre fazla iletirler.
- Tel ve levha haline getirilebilirler.
- Elektronik devrelerde, Mercek ve projektörlerde kullanılırlar.
Bu konu anlatımının çalışma kağıdına ulaşmak için buraya tıklayabilirsiniz.
Böylelikle Periyodik Tablo konusunu tamamladık. Umuyoruz ki bu konuyu yararlı bulmuşsunuzdur.
Güncel konular için facebook , instagram ve google+ üzerinden bizi takip edebilirsiniz. Tekrar görüşmek üzere.


Çok güzel anlatmışsınız 😃